镁合金是目前密度最小的金属工程材料,资源丰富、比强度高及减震性能好等优点使其跻身轻量化领域[1],节能利于成本降低;但强度、塑性不佳限制了其推广应用。近年来,Mg-RE 合金研发势头迅猛,Mg-Gd-Zn 合金因优良力学性能备受关注。此外,晶粒细化是进一步改善镁合金力学性能的常用方法。目前,镁合金块体和粉末晶粒细化的途径为:前者在熔炼凝固过程中提高形核率及抑制晶粒长大速度或成形后经由大塑性变形得到成型细晶材料,包括添加形核剂[2]、等通道转角挤压[3]、累积叠轧[4-5]、高压扭转[6]等,细化极限为0.5~1.0 μm;后者先制备细晶粉末后固结形成块材,主要包括高能球磨、雾化法等,可将晶粒细化至纳米级。
氢化-歧化-脱氢-重组(Hydrogenation-Disproportionation-Desorption-Recombination,HDDR)作为一种新型且有效的晶粒细化技术,最初由Takeshita和Nakayama 提出[7],Harris 团队[8-9]首次将其应用于Nd-Fe-B 系磁性材料。此后不断推广实践,先后开展对TiAl[10]、AZ31[11-12]、Mg-3Ni-2MnO2[13]、AZ91[14]、ZK60[15]及Mg[16]的研究,并实现很好的细化效果。Takamura等[11]通过对AZ31 粉末及板材进行HDDR 处理,结果表明粉末由微米晶细化至纳米晶;板材经36 h 处理,晶粒尺寸减小到500 nm 以下,氢化层渗透了约20 μm。Hu 等[12]将氢气与机械力相结合处理AZ31铸态粉末后脱氢制备了40~50 nm 的粉末。目前,已经证明HDDR 对AZ 及ZK 系镁合金具有很好的细化作用,但对GZ 系合金是否具有相同的细化效果相关文献很少。本文采用HDDR 工艺处理球磨GZ132K 镁合金粉末,研究其相转变和组织形貌演变过程及细化机理。
1 实验材料与方法
实验初始材料为球磨GZ132K 镁合金粉末,其名义成分与实际成分如表1 所示。每次称取2 g 置于改造的高温高压反应釜中,抽真空2 h 后充入一定量高纯氢气,通过保压测试后升温至目标温度开始氢化。通过改变温度(300、350 和400 ℃)、氢压(2、3 和4 MPa)和时间(8、12 和18 h),设计氢化正交试验。脱氢时,放入约1 g 最佳氢化条件下制备的氢化粉抽真空2 h 后,分别升温至300、350 和400 ℃真空脱氢6 h。
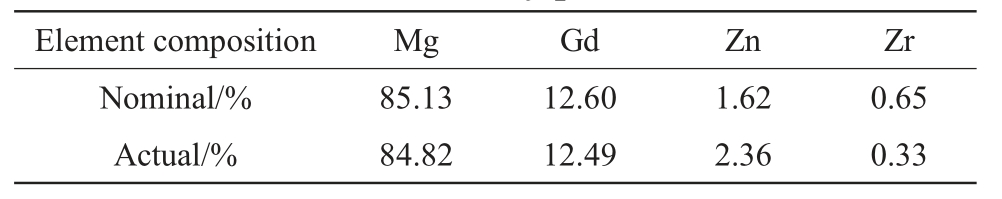
表1 球磨GZ132K镁合金粉末名义成分与实际成分
Tab.1 Nominal and actual composition of ball milled GZ132K alloy powder
各样品物相通过DX-2700 SSC 型号X 射线衍射仪测定,以Cu-Kα 为靶材,连续扫描采集数据点,扫描起始角和终止角为20°和80°,扫描速度4(°)/min,步长0.01°。样品表面形貌通过JSM-6700F场发射扫描电镜观察。晶粒大小及选区电子衍射利用JEM-2100F 场发射透射电子显微镜表征。
2 实验结果及讨论
2.1 XRD 分析
图1 是原始及氢化样品的XRD 图谱。图1(a)为原始样品及1#、2#和3#样品的XRD 图谱,可以看到,原始粉末由α-Mg、Mg5Gd 及Mg-Zn-Gd 3 相组成。在300 ℃氢化,合金相Mg-Zn-Gd 和Mg5Gd在加热过程中由于热不稳定性发生了分解,反应后物相转变为α-Mg、Mg2Gd 及β-Gd。3 组样品中均未观察到氢化物生成,这说明在300 ℃及以下温度,无法提供足够的激活能,使得GZ132K 粉末中的金属原子与H2 发生反应形成金属氢化物,即使增大氢压或延长氢化时间都无所助益。
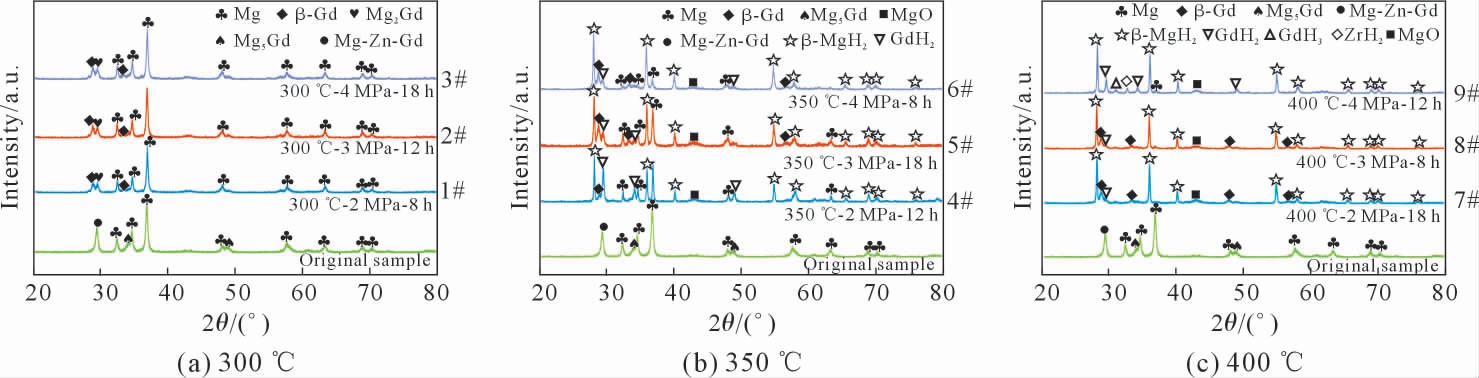
图1 原始样品及氢化样品的XRD 图谱
Fig.1 XRD patterns of original and hydrogenated samples
4#、5#和6#为350 ℃氢化的试样,由图1(b)可知,3 组样品氢化后不同程度的生成了MgH2 及GdH2,说明350 ℃已经满足氢化反应的热力学条件,同时也进一步证明了GZ132K 合金粉末有氢化的可能性。但在该温度任何条件下,样品都只表现为部分氢化,还有残存的单相α-Mg 及β-Gd。
当温度升高至400 ℃时,如图1(c)所示,7#和8 # 样品中的α-Mg 相完全转变形成MgH2,9 #样品中残存一个衍射强度极低的Mg 峰,对主相Mg而言,氢化效果显著。但注意到β-Gd 氢化动力学缓慢且条件苛刻,只有在4 MPa 氢压下反应12 h 才能实现完全氢化,此时表现为GdH2 与GdH3 共存;在该条件下,还存在一个ZrH2 的衍射峰。
基于上述9 组XRD 图谱中不存在无定型弥散峰,且每一物相的K 值可从标准PDF 卡片获悉,根据绝热法[17]计算各相的质量分数,并将氢化物质量分数之和记为氢化率,汇编于表2 并做极差分析,可以得出结论:温度是氢化率的主要影响因素,氢压次之,时间与交互作用极差值相差很小难以确定影响的先后顺序。而在本实验条件下,温度升高,氢化率不断增加;2、3 MPa 氢压对氢化率影响很小,基于β-Gd 氢化时完全转变为其氢化物条件苛刻,选择4 MPa、12 h 作为GZ132K 镁合金粉末氢化反应氢压和时间。下面针对温度对氢化程度影响进行实验。
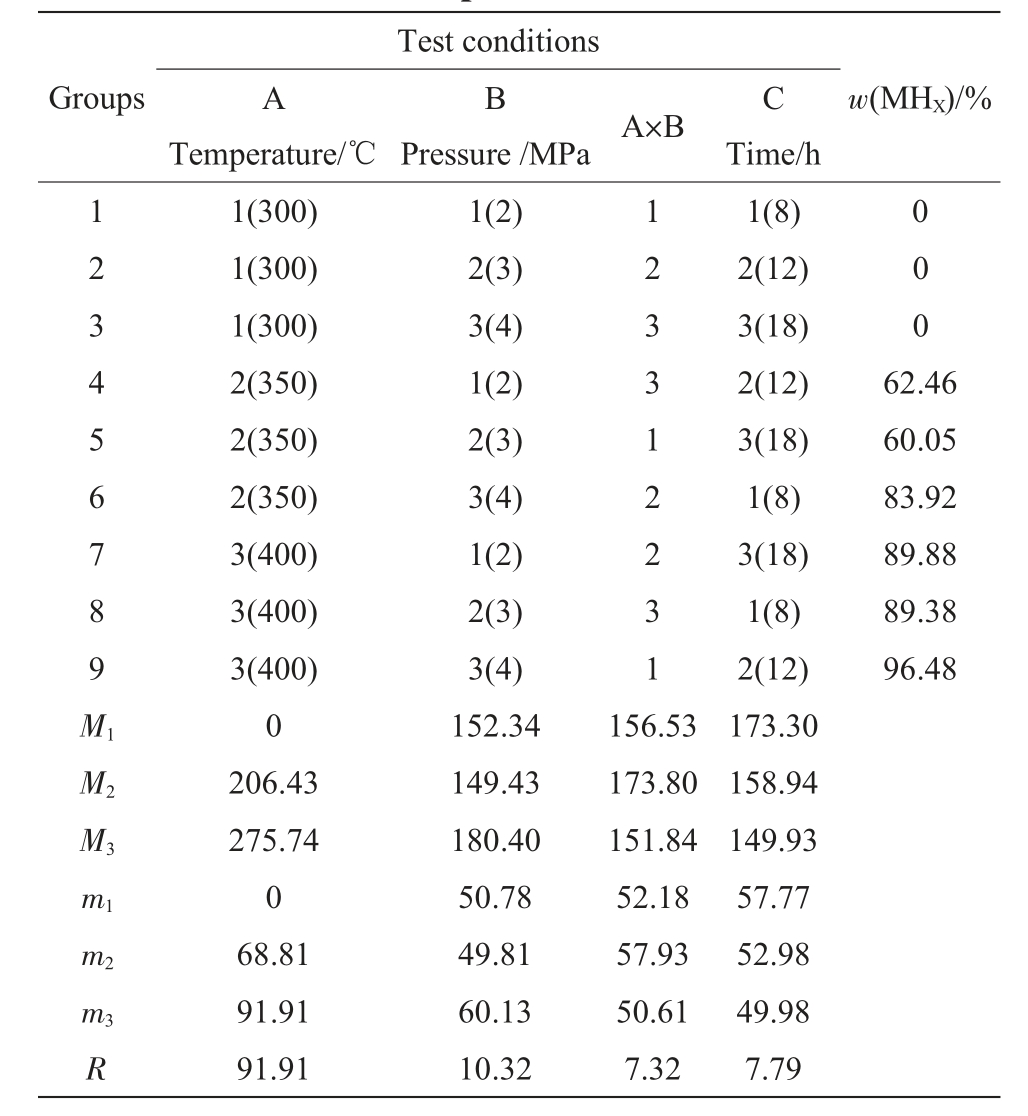
表2 氢化正交试验结果与分析
Tab.2 Results and analysis of orthogonal hydrogenation process
初始粉末在4 MPa 氢压下,分别在350、400 和450 ℃氢化12 h 的XRD 图谱如图2 所示。当反应温度为350 ℃时,大部分Mg 发生了向MgH2 的相转变,同时三元化合物Mg-Zn-Gd 分解,有β-Gd 和GdH2 生成,说明该温度已满足MgH2、GdH2 生成的热力学条件。400 ℃时,除一个衍射强度不太显著的Mg 峰外,其余全部为氢化物;Gd 的氢化物主要是GdH2,伴随少量GdH3。温度进一步升高到450 ℃,Mg 已全部转换为MgH2,但Gd 的氢化物GdH2 几乎全部消失,出现了β-Gd 和GdH3。这说明对于β-Gd 氢化反应存在一个合适的温度,当低于350 ℃时,由于温度低不能提供足够的激活能,只有部分原子被氢化;而高于450 ℃进行反应时,高温造成正反应处于被抑制状态,也不利于氢化反应。此外,随着反应温度的增加,Gd 的氢化物从GdH2向GdH3 转化。基于上述分析,将400 ℃作为氢化反应温度。
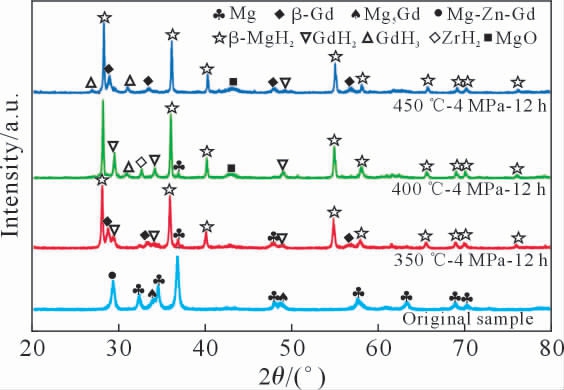
图2 GZ132K 粉末分别在4 MPa 氢压下,350、400 和450 ℃氢化12 h 的XRD 图谱
Fig.2 XRD pattern of GZ132K powder hydrogenated at 350,400 and 450 ℃under 4 MPa hydrogen pressure for 12 h
综合确定球磨GZ132K 镁合金粉末的氢化条件为:400 ℃、4 MPa 氢压下氢化12 h。重复试验3次,平均氢化率达97%。依据XRD 图谱对MgH2 进行晶格常数估算:a=0.451 6 nm,c=0.302 1 nm,这一结果比标准卡片(PDF#01-075-794 4)常数稍大,后者a=0.451 5 nm,c=0.301 9 nm,猜测可能是H 原子过饱和固溶于间隙位置处,导致晶格膨胀。
由于氢化反应在300 ℃难以启动,而脱氢反应作为氢化的逆过程,故脱氢温度选择从350 ℃开始。脱氢的原材料为最佳氢化条件下制备的GZ132K 氢化粉,图3 是氢化粉分别在350、400 和450 ℃真空脱氢6 h 的XRD 图谱。350 ℃,脱氢开始,但只是部分脱氢;升温至400 ℃,物相组成与350 ℃生成物一致,MgH2 分解量稍有增加,说明在相同脱氢时间下,温度越高脱氢速率越快。继续升温至450 ℃,MgH2 完全分解,物相组成仅为α-Mg 和β-Gd。升高温度主要从两方面促进脱氢反应进行:其一,高温抑制氢化反应,作为吸收热量的脱氢反应,温度升高可为其提供更多激活能,满足热力学条件;其二,升温原子扩散速率及化学反应速率都会增加,显著提升动力学条件。
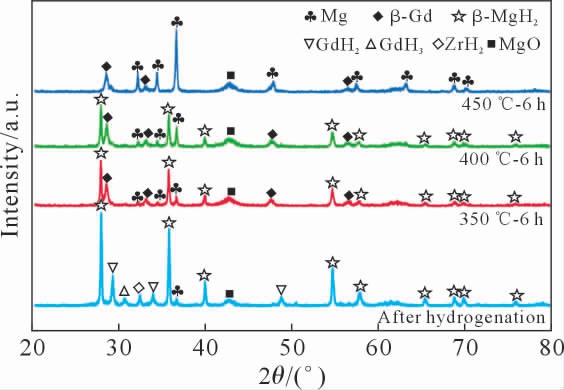
图3 GZ132K 氢化粉分别在350、400 和450 ℃脱氢6 h 的XRD 图谱
Fig.3 XRD pattern of hydrogenated GZ132K powder dehydrogenated at 350,400 and 450 ℃for 6 h
对在450 ℃持续抽取真空6 h 的脱氢试样中的α-Mg 相进行晶格常数估算,结果为a=0.321 3 nm,c=0.5217 nm,与标准Mg 相(PDF#04-007-384 7)的晶格常数(a=0.321 3 nm,c=0.521 3 nm)在误差范围内保持一致。根据物相组成及晶格常数,可认为氢化GZ132K 粉末在该条件下已实现完全脱氢,故而选定脱氢条件为:450 ℃持续真空脱氢6 h。
2.2 SEM 分析
初始粉末、400 ℃、4 MPa 氢压下氢化12 h 的氢化粉及在450 ℃持续脱氢6 h 脱氢粉3 组样品表观形貌如图4 所示。图4(a)是初始粉末形貌,颗粒外缘钝化表面平整,单个颗粒表现为复合层片状,对约150 个颗粒统计,可得到结论:颗粒大小不均匀,长度方向粒径约3~26 μm,平均粒径为10 μm。氢化物形貌如图4(b)所示,颗粒体积膨胀增大,表面呈现毛絮团状并伴随碎屑状小颗粒粘附,与此同时生出裂纹。依据标准PDF 卡片,Mg 单胞体积为4.659 nm3,MgH2 单胞体积为6.154 nm3,当Mg 转变为MgH2时,单胞体积膨胀约32%,氢化过程中H 原子通过缺陷和体扩散进入晶格并使之膨胀,受邻近晶粒约束阻挡造成氢爆或产生内应力,导致裂缝萌生,图中箭头所指为裂纹;而且MgH2 较脆,裂纹不断延伸扩展,大颗粒逐步破碎成小颗粒。脱氢后毛絮团状形貌及裂纹消失,颗粒尺寸无明显变化,其形貌如图4(c)所示。

图4 HDDR 过程中GZ132K 粉末SEM 图
Fig.4 SEM images of GZ132K alloy powder in HDDR process
2.3 TEM 分析
图5 (a~c) 显示初始粉末晶粒分布极不均匀,尺寸范围为12~76 nm,平均晶粒尺寸约40 nm。图5(c~i)为氢化-脱氢过程中合金的TEM 及其晶粒尺寸分布图,看到氢化物的平均晶粒尺寸约22 nm,脱氢后平均晶粒尺寸进一步细化至约9 nm,可见氢化-脱氢处理能够明显且持续细化球磨GZ132K 镁合金,氢化过程中细化程度更大些,脱氢过程中较小程度细化但晶粒尺寸更加均匀。
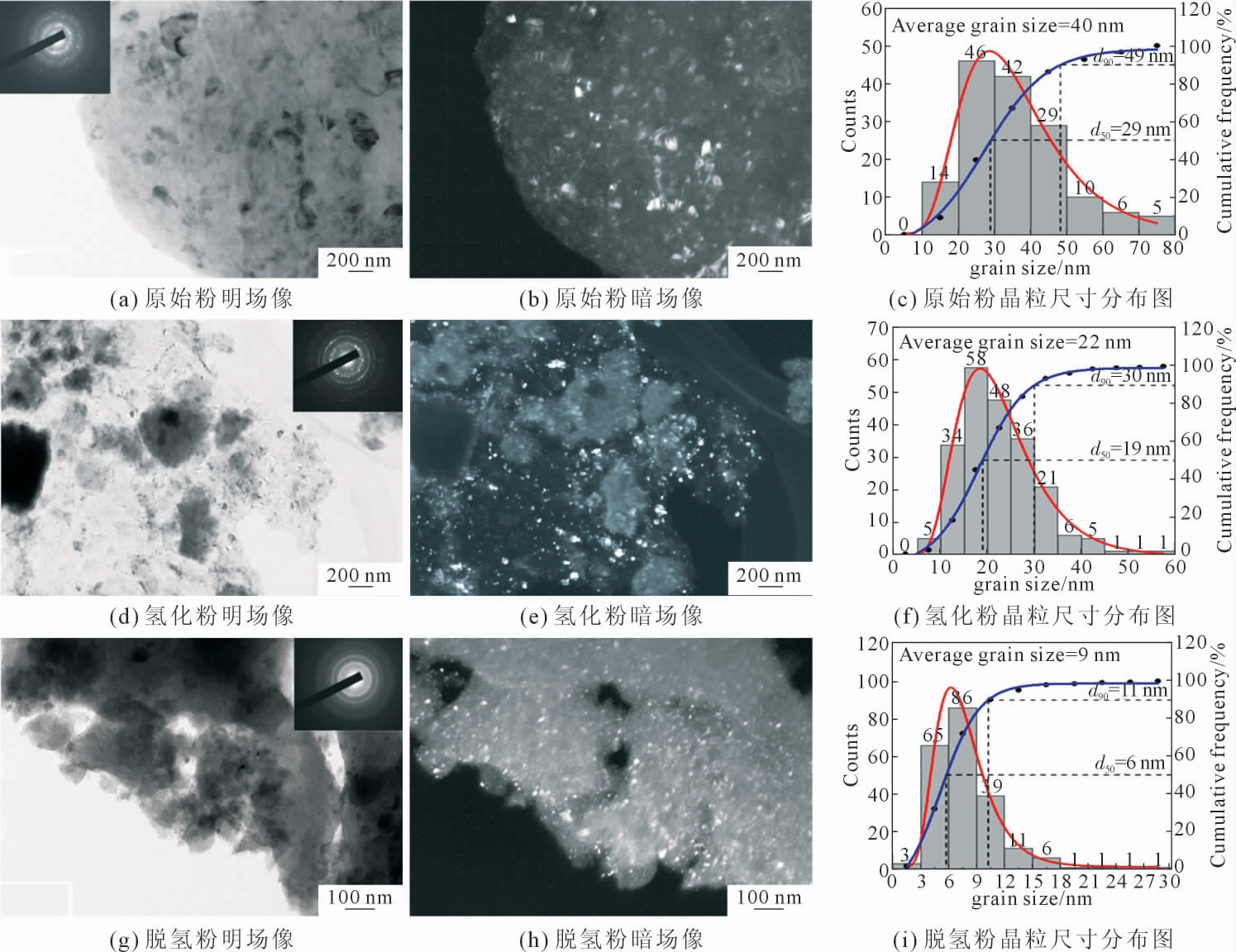
图5 原始、氢化及脱氢GZ132K 镁合金粉末的TEM 及晶粒尺寸分布图
Fig.5 TEM images and grain size distribution of original,hydrogenated and dehydrogenated GZ132K alloy powder
2.4 细化机理分析
根据上述分析可知,初始材料中的合金相Mg-Zn-Gd 及Mg5Gd 在氢化过程中先分解形成Mg及β-Gd 后,与H2 反应形成其氢化物,但脱氢后未能实现重组,因此,球磨GZ132K 镁合金的HDDR过程可认为是Mg 及Gd 的氢化物的化合与分解过程。
球磨后金属颗粒大部分已被破碎成趋规则状小颗粒,但仍有很小部分表现为近球形,氢化-脱氢时,前者比后者具有更快更优的反应动力学条件,在此处以近球形主相Mg 颗粒的反应过程进行分析。球磨后Mg 颗粒具有多种缺陷,结合气固反应理论,以及Mg 向MgH2 转变时单胞体积膨胀约32%的事实;依托于未反应核的模型,进一步改进其反应模型,当在400 ℃及4 MPa 氢压下主要分为以下步骤进行氢化反应,如图6 所示。
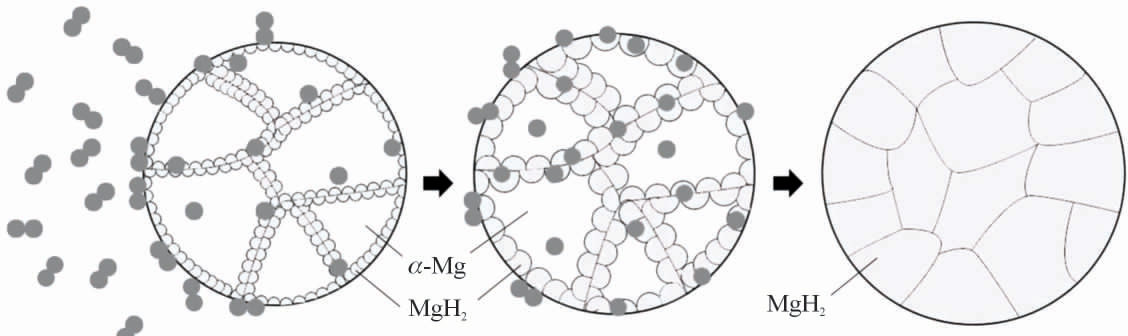
图6 氢化反应示意图
Fig.6 Schematic diagram of hydrogenation reaction
(1)H2 主流体气相传质到Mg 颗粒附近并在表面物理吸附。
(2)在热驱动下,H2 分解成为H 原子,部分沿缺陷快速扩散,部分在Mg 颗粒表面化学吸附。
(3)H 原子扩散进入Mg 间隙,形成Mg(H)过饱和固溶体后形核并长大,形成MgH2。
(4)H 原子持续渗透穿过MgH2 层化学反应继续,直至完全转换成MgH2,反应结束。
球磨后内部缺陷增多,MgH2 优先在缺陷及表面形核,因此形核率提高,利于晶粒细化。另一方面MgH2 为脆性相易破碎,因此,氢化后,平均40 nm的原始晶粒细化至22 nm。但研究[18]表明,H 原子在Mg 中的扩散速率高过MgH2 约3~4 个数量级,后续H 原子在氢化层中扩散困难,影响氢化进程,因此在本实验中需要12 h 才能实现完全氢化。
脱氢则是氢化的逆反应过程,氢化反应结束后,颗粒表面出现裂纹,为H 原子从颗粒中脱出提供极速通道,此时表面脱氢同步进行。MgH2 在450 ℃转变为不稳定相结构,H 原子因热振动脱离原来位置,转变成Mg(H)固溶体,随后在热驱动下不断从固溶体间隙中扩散,穿过脱氢产物层,在真空持续抽取状态下,重新结合成为H2 被排出系统外;与此同时,Mg 原子在表面及缺陷处形核并长大,历经6 h 最终还原成Mg,此时平均晶粒尺寸约9 nm。脱氢过程如图7 所示。
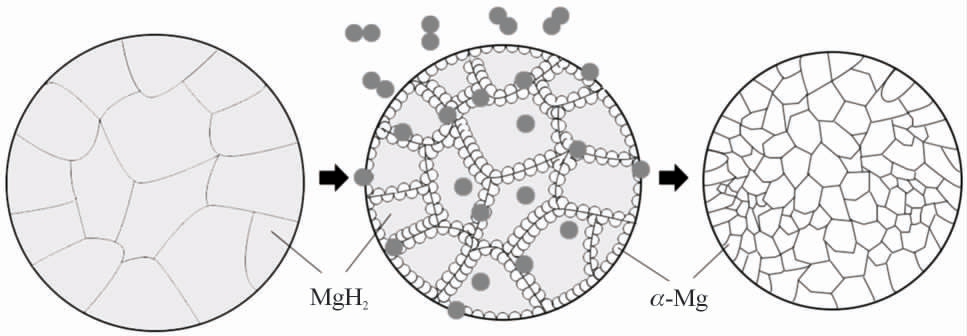
图7 脱氢反应示意图
Fig.7 Schematic diagram of dehydrogenation reaction
3 结论
(1)球磨GZ132K 镁合金粉末最佳HDDR 工艺参数为:400 ℃,4 MPa 氢压下氢化12 h,随后再450 ℃持续真空脱氢6 h。
(2)通过HDDR 处理,球磨GZ132K 镁合金粉末由12~76 nm 原始晶粒细化至平均约9 nm 的均匀纳米晶,具有显著细化效果。
(3)球磨GZ132K 镁合金的HDDR 过程可认为是Mg 及Gd 氢化物的化合与分解过程。
[1]徐河,刘静安,谢水生.镁合金制备与加工技术[M].北京:冶金工业出版社,2007.
[2]XING F J,GUO F,SU J,et al.The existing forms of Zr in Mg-Zn-Zr magnesium alloys and its grain refinement mechanism[J].Materials Research Express,2021,8(6):066516.
[3]SEGAL V M,REZNIKOV V I,DROBYSHEVSKIY A E,et al.Plastic working of metals by simple shear[J].Russian Metallurgy,1981,19(1):99-105.
[4]SAITO Y,UTSUNOMIYA H,TSUJI N,et al.Novel ultra-high straining process for bulk materials-development of the accumulative roll-bonding (ARB) process[J].Acta Materialia,1999,47(2):579-583.
[5]KUMAR P,MADHUP A,KALVALA P R,et al.Texture evaluation in AZ31/AZ31 multilayer and AZ31/AA5068 laminar composite during accumulative roll bonding[J].Defence Technology,2020,16(3):514-519.
[6]ZHILYAEV A P,LANGDON T G.Using high-pressure torsion for metal processing: Fundamentals and applications[J].Progress in Materials Science,2008,53(6):893-979.
[7]TAKESHITA T,NAKAYAMA R.Proceedings of the 10 th International workshop on rare-earth magnets and their applications[M].Kyoto,1989.
[8]BOOK D,HARRIS I R.The disproportionation of Nd2Fe14B under hydrogen in Nd-Fe-B alloys[J].IEEE Transactions on Magnetics,1992,28(5):2145-2147.
[9]BOOK D,HARRIS I R.Hydrogen absorption/desorption and HDDR studies on Nd16Fe76B8 and Nd11.8Fe82.3B5.9[J].Journal of Alloys and Compounds,1995,211(1-2):187-192.
[10]AOKI K,ITOH Y,MASUMOTO.Preparation of nanocrystallineTiAl powder by the HDDR process using mechanical grinding in a hydrogen atmosphere[J].Scripta Metallurgica Et Materialia,1994,31(9):1271-1275.
[11]TAKAMURA H,MIYASHITA T,KAMEGAWA A.Grain size refinement in Mg-Al-based alloy by hydrogen treatment[J].Journal of Alloy and Compounds,2003,356:804-808.
[12]HU L X,YANG W,YUAN Y,et al.Microstructure nanocrystallization of a Mg-3%Al-1%Zn alloy by mechanically assisted hy driding-dehydriding[J].Materials Letters,2008,62(17-18):2984-2987.
[13]FANG W,SUN H F,FANG W B.Effcet of Al and Zn additives on grain size of Mg-3Ni-2MnO2 alloy[J].Transactions of Nonferrous Metals Society of China,2009,19(S2):355-358.
[14]LIU Y F,FANG J F,ZHANG H,et al.Formation and mechanism of nanicrystalline AZ91 powders during HDDR processing[J].Materials Characterization,2017,125:131-141.
[15]许联林,樊建锋,张华,等.氢化-脱氢制备ZK60 纳米晶镁合金材料及组织演化[J].稀有金属材料与工程,2017,46(10):2908-2913.
[16]郭卉君.块体纳米晶纯镁的微观组织的稳定性及力学性能研究[D].太原:太原理工大学,2018.
[17]周玉.材料分析方法(第三版)[M].北京:机械工程出版社,2017.
[18]TO¨PLER J,BUCHNER H,SA¨UFFERER H,et al.Measurements of the diffusion of hydrogen atoms in magnesium and Mg2Ni by neutron scattering[J].Journal of the Less Common Metals,1982,88(2):397-404.